Les
espèces chimiques, telles que les principes actifs des médicaments,
peuvent être d'origine naturelle ou créées par l'Homme. Le plus souvent
elles sont mélangées à d'autres espèces et il est donc nécessaire de les
séparer. En fonction de leur état physique et de leurs propriétés
chimiques plusieurs techniques sont possibles. On utilise aussi
certaines de ces caractéristiques pour les identifier.
I
Les origines des espèces chimiques
Espèce chimique naturelle
Une espèce chimique naturelle est une espèce qui est issue de la nature (de végétaux, animaux ou minéraux).
Le sucre (saccharose) est une espèce chimique naturelle pouvant être extraite de la canne à sucre ou de la betterave.
Espèce chimique synthétique
Une espèce chimique synthétique (ou de synthèse) est fabriquée par l'Homme en laboratoire à l'aide de transformations chimiques.
Le Nylon est une fibre textile créée par l'industrie chimique.
Certaines
espèces chimiques synthétiques sont identiques à des espèces
naturelles, alors que d'autres n'existaient pas avant que les chimistes
les créent, on dit qu'elles sont artificielles.
La vitamine C peut être extraite de produits naturels (agrumes, etc.) ou préparée dans un laboratoire.
L'aspartame
est une molécule qui n'existe pas dans la nature, elle a été créée par
l'Homme : c'est donc une molécule artificielle.
II
Les propriétés permettant la séparation d'espèces chimiques
A
La miscibilité et la densité des liquides
Miscibilité
La miscibilité est la capacité de deux liquides à se mélanger.
L'eau
et l'éthanol sont deux liquides miscibles en toutes proportions alors
que l'eau et l'huile sont deux liquides non miscibles.
- Si les deux liquides sont miscibles, leur mélange est constitué d'une seule phase ("partie"), on dit qu'il est homogène.
- Si les deux liquides sont non miscibles, leur mélange est constitué de deux phases, on dit qu'il est hétérogène.
Densité
La densité d d'un corps est le rapport de sa masse volumique par celle de l'eau :
dcorps=μcorpsμeau , avec μeau=1 kg.L−1
C'est une grandeur sans unité (les deux masses volumiques devant être exprimées avec la même unité).
C'est une grandeur sans unité (les deux masses volumiques devant être exprimées avec la même unité).
La masse volumique d'une huile d'olive est ρhuile=0,92 kg.L−1, sa densité est donc :
dhuile=μhuileμeau=0,921=0,92 .
L'huile d'olive étant moins dense que l'eau, dans une ampoule à décanter elle se place au-dessus.

Position des phases dans une ampoule à décanter
On appelle :
- "Phase aqueuse" : la phase dans laquelle le solvant est l'eau.
- "Phase organique" : la deuxième phase, car généralement elle est composée d'un solvant organique.
B
La solubilité d'une espèce chimique dans un solvant
Solubilité
La
solubilité d'un soluté est la concentration maximale de ce composé que
l'on peut dissoudre dans un solvant et à une température donnée.
A 20°C, la solubilité du sel (chlorure de sodium) dans l'eau est de 360 g.L−1.
On peut donc dissoudre au maximum 360 g de sel dans 1 L d'eau, au-delà
la solution est saturée et le sel ajouté se dépose au fond du récipient.
Ainsi,
en fonction de sa solubilité une espèce chimique peut se dissoudre plus
ou moins bien dans un solvant. Lorsqu'elle ne peut plus se dissoudre,
on dit que la solution est saturée.
III
Les techniques d'extraction
A
La filtration
Filtration
La
filtration permet de séparer les espèces chimiques d'un mélange solide −
liquide par passage à travers un filtre. On appelle filtrat le liquide
filtré et résidu le solide retenu.

Montage de filtration
Pour
augmenter la rapidité et l'efficacité de la filtration, il est possible
de l'effectuer sous pression réduite, avec un filtre Büchner.
B
L'hydrodistillation
L'hydrodistillation
L'hydrodistillation
est une technique permettant d'extraire des espèces chimiques volatiles
contenues dans un produit naturel (plantes, feuilles, écorces, etc.) en
le faisant bouillir dans l'eau. Le mélange des vapeurs d'eau et d'huile
essentielle est ensuite condensé (rendu liquide) par un réfrigérant.
On
peut extraire l'huile essentielle de lavande en faisant subir une
hydrodistillation à un mélange d'eau et de fleurs de lavande.
L'hydrodistillation
repose sur le fait que même si l'huile essentielle et l'eau ne sont pas
miscibles à l'état liquide, elles le deviennent à l'état gazeux.
Le
mélange obtenu contient l'huile essentielle et l'eau. Ces deux liquides
étant généralement non miscibles, on les sépare ensuite en utilisant
une ampoule à décanter.
C
L'extraction par solvant (ou extraction liquide − liquide)
Extraction par solvant
L'extraction
par solvant (ou extraction liquide − liquide) permet d'extraire une
espèce chimique dissoute dans un solvant, à l'aide d'un autre solvant,
appelé solvant d'extraction, dans lequel elle est plus soluble. Le
solvant initial et le solvant d'extraction ne doivent pas être
miscibles, ce qui permet de les séparer en utilisant une ampoule à
décanter.

Les trois étapes d'une extraction par solvant
En
choisissant un solvant extracteur qui soit en plus volatil, il sera
facile de l'éliminer (en l'évaporant) et d'isoler l'espèce chimique qui a
été extraite.
D
D'autres techniques d'extraction
Il existe d'autres techniques d'extraction, parfois très anciennes :
- Le pressage : obtention des produits par pression (exemple : extraction de l'huile d'olive).
- L'enfleurage : on dépose la substance naturelle sur de la graisse (exemple : extraction des espèces odorantes des fleurs fragiles).
- La macération : la substance naturelle est mélangée à un solvant, à froid (exemple : macération de fruits dans de l'alcool).
- L'infusion : on verse de l'eau bouillante sur la plante hachée (exemple : préparation de thé).
- La décoction : on fait cuire la plante, au moins plusieurs minutes, dans de l'eau bouillante (exemple : préparation du café turc).
IV
La séparation d'espèces chimiques : chromatographie sur couche mince (ou CCM)
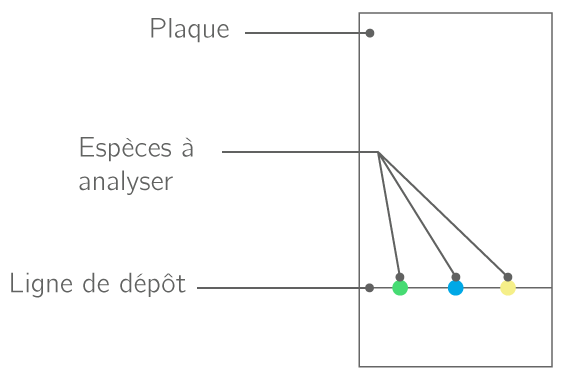
La
chromatographie sur couche mince (CCM) permet d'identifier les
différents constituants d'une solution. On dispose d'une plaque, sur
laquelle on dispose, sur une seule ligne, une goutte de chaque solution à
analyser :
Chromatographie sur couche mince
La
chromatographie sur couche mince est une méthode physique permettant de
séparer et d'identifier des espèces chimiques présentes dans un mélange
de liquides homogènes. Elle est basée sur les différences d'affinité
des espèces chimiques étudiées entre la phase fixe (le papier) et la
phase mobile, appelée éluant.
On dépose sur une plaque de papier, sur une seule ligne appelée "ligne de dépôt", une goutte de chaque liquide à analyser :
On
place ensuite cette plaque dans un bécher contenant l'éluant. Celui-ci
va entraîner chaque espèce chimique à des vitesses différentes :
Chromatogramme
Le
chromatogramme est le résultat de la chromatographie. Les espèces
chimiques sont caractérisées par les hauteurs qu'elles ont atteintes
lors de l'élution.
Le
chromatogramme suivant montre que le mélange vert est composé d'une
espèce chimique donnant une couleur jaune et d'une autre donnant une
couleur cyan.

Chromatogramme
On caractérise notamment les espèces chimiques par leur rapport frontal Rf qui ne dépend que de la phase fixe et de l'éluant.
Rapport frontal
Le rapport frontal Rf d'une espèce dans un chromatogramme est définie par :
Rf=Distance parcourue par l'espèce chimiqueDistance parcourue par le front de l'éluant=hH
L'espèce
chimique donnant la couleur jaune dans le mélange vert est la même que
celle déposée à côté car leurs rapports frontaux sont identiques.

Grandeurs permettant de calculer le rapport frontal du colorant jaune
V
L'identification d'une espèce chimique
A
A partir de ses caractéristiques physiques ou chimiques
Toute
espèce chimique possède des propriétés physiques dont les valeurs lui
sont propres, on les nomme caractéristiques physiques. Elles permettent
de l'identifier :
Les valeurs attendues peuvent dépendre d'autres paramètres qu'il faut préciser, comme la pression, la température, etc.
Une faible variation autour de la valeur attendue met en évidence la présence d'impuretés.
| Caractéristiques | Mesure |
|---|---|
| Température de changement détat |
|
| Densité |
|
| Indice de réfraction |
|
| Solubilité |
|
Une faible variation autour de la valeur attendue met en évidence la présence d'impuretés.
A 20°C, l'indice de réfraction de l'eau pure est 1,330 mais il augmente si l'eau contient du sel par exemple.
B
A partir d'une chromatographie sur couche mince
On
peut identifier une espèce chimique en réalisant une chromatographie
sur couche mince avec des échantillons de référence. Les espèces de
mêmes rapports frontaux sont identiques.
Pour
identifier les espèces chimiques composant l'huile essentielle obtenue
après hydrodistillation de feuilles de menthe, on réalise la
chromatographie suivante :

Chromatographie de l'huile essentielle obtenue après hydrodistillation des feuilles de menthe
La
comparaison des différentes taches montre que l'huile essentielle
obtenue contient de la menthone, du menthol, du menthofurane mais pas
d'eucalyptol.
Extraction, séparation et identification d'espèces chimiques (La santé, Le sport)
4/
5
Oleh
dirassa